Nieuw mechanisme onthult de reactie van kooldioxide aan het oppervlak van water
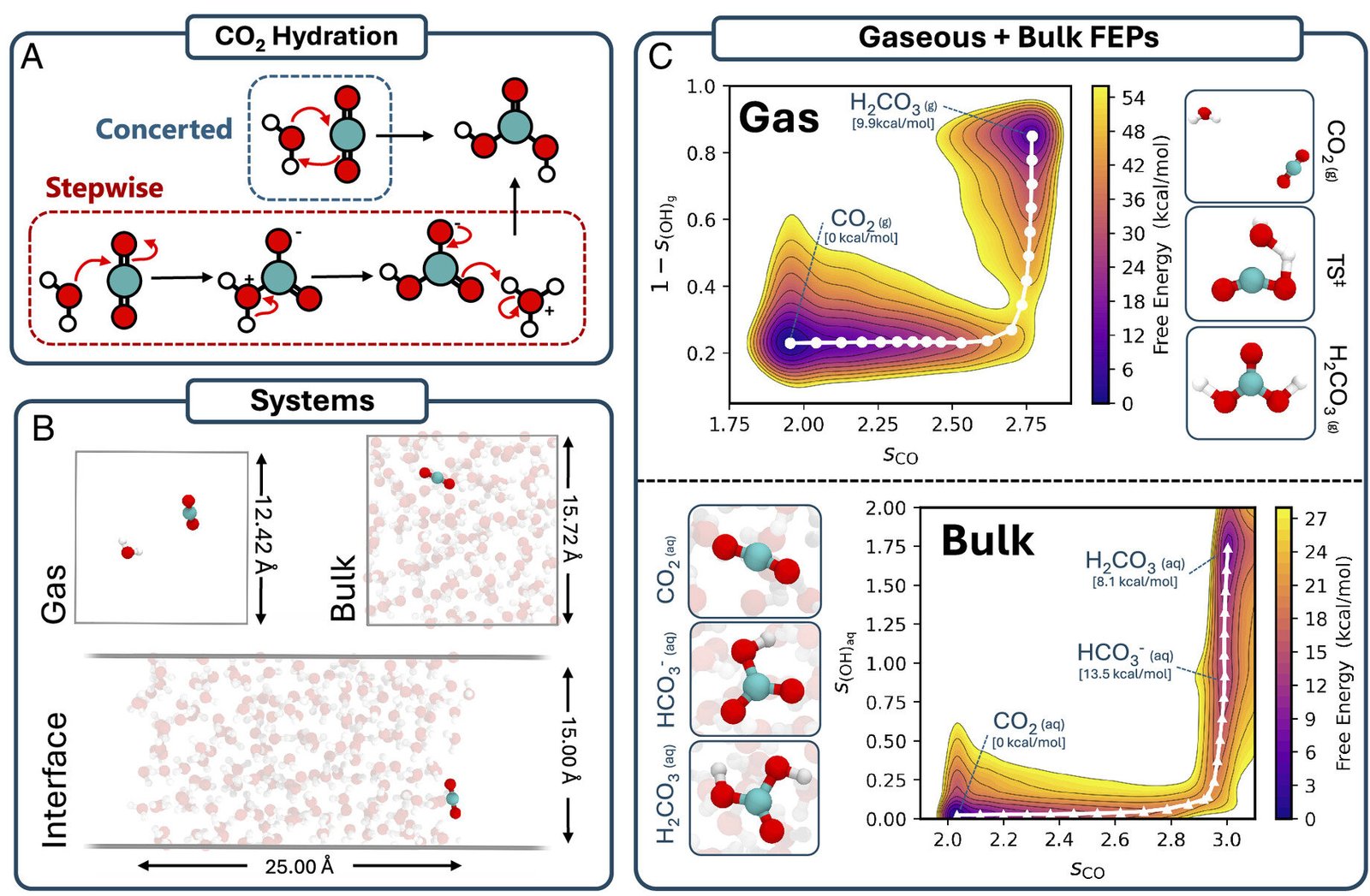
Modeling van de CO2 + H2O-reactie door middel van verbeterde steekproef moleculaire simulaties.
Elk jaar worden er miljarden tonnen CO2 in de atmosfeer gepompt. Een aanzienlijk deel hiervan komt in de oceanen van de aarde terecht, waar het kan reageren met water om koolzuur (H2CO3) te vormen, wat leidt tot verzuring van de oceanen.
Hoewel veel onderzoek zich heeft gericht op hoe dit proces diep in de vloeistof plaatsvindt, is er minder aandacht geweest voor hoe deze reactie verloopt aan waterige interfaces, waar water een andere stof ontmoet, bijvoorbeeld aan het oceaanoppervlak.
In een studie hebben onderzoekers van de Universiteit van Cambridge en University College London ontdekt dat CO₂ kan reageren binnen de bovenste laag water, via een nieuw “in en uit” mechanisme. In dit proces, in plaats van volledig op te lossen in het water, doopt CO₂ kort in de oppervlaktelaag, reageert en komt dan weer naar boven. Dit gebeurt in een zeer dunne laag, slechts enkele moleculen dik.
“Het is alsof CO₂, in plaats van diep in het water te duiken om te reageren, een snelle duik in het water neemt, gedeeltelijk oplost in de bovenste laag waar het kan reageren om koolzuur te vormen. Deze zuursoort komt vervolgens terug naar het oppervlak en verschijnt weer,” zei Samuel Brookes, eerste auteur van het artikel en Ph.D. student aan het Yusuf Hamied Department of Chemistry en het Cavendish Laboratory van Cambridge.
Het in en uit mechanisme daagt eerdere aannames uit over waar en hoe CO₂ kan veranderen in koolzuur en toont aan dat reacties kunnen plaatsvinden direct aan het wateroppervlak, niet alleen diep erin.
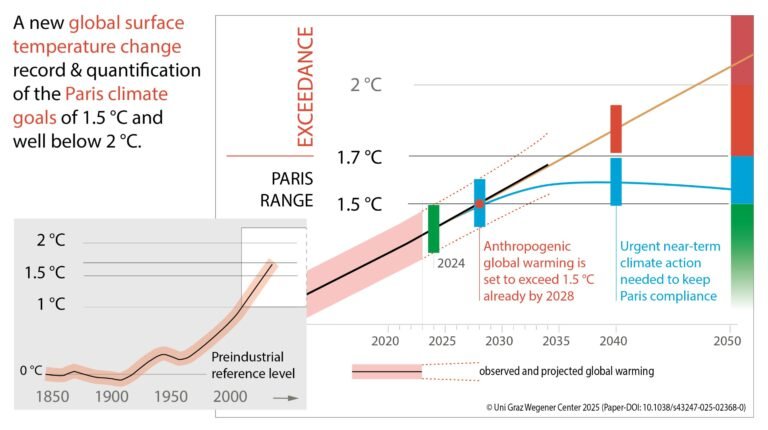
Het begrijpen van hoe CO₂ reageert aan het wateroppervlak is cruciaal voor het verbeteren van klimaatmodellen en voorspellingen.
Wetenschappers weten uit eerdere studies dat grote hoeveelheden CO₂ zich aan het oceaanoppervlak verzamelen. Nu suggereert het Cambridge-team dat dit oppervlak CO₂ niet volledig hoeft op te lossen voordat het reageert. In plaats daarvan kan het reageren op de plek waar het zich bevindt, wat betekent dat oceanische verzuring sneller kan gebeuren dan eerder gedacht.
“Helaas suggereert dit dat huidige voorspellingen over veranderingen in de pH van de oceaan, die de zuurgraad meet, mogelijk onderschat zijn,” zei Brookes. “Dit maakt de noodzaak voor nauwkeurige klimaatmodellen nog dringender.”
De wetenschappers maakten gebruik van machine learning om dit verzuringsproces aan de lucht-waterinterface te bestuderen. De modellen, getraind op nauwkeurige gegevens op kwantumniveau, stelden hen in staat om de reactie op het niveau van atomen en moleculen te simuleren. Van deze waarnemingen op moleculair niveau konden de onderzoekers vervolgens betekenisvolle voorspellingen doen, zoals reactiekrachten en -paden.
Onderzoekers waren verrast door de gelijkenis tussen de reactie aan de interface en in bulkoplossing. Ze verwachtten dat de reactie om koolzuur te vormen veel moeilijker zou zijn aan het wateroppervlak dan dieper in het water vanwege het lagere aantal beschikbare watermoleculen, wat chemische reacties moeilijker kan maken.
“Maar vanwege dit in en uit mechanisme ontdekten we dat het gebrek aan omringende watermoleculen aan het oppervlak de reactie niet moeilijker maakte, zoals we aanvankelijk hadden voorspeld, en de energie die nodig was om koolzuur te vormen, was ongeveer hetzelfde aan het oppervlak als dieper in het water,” zei Brookes.
Nadat ze het onderliggende reactiemechanisme hadden onthuld, waren de onderzoekers ook gefascineerd door hoeveel de reactiekenmerken veranderden over zo’n korte afstand. “Door CO₂ slechts een fractie van een nanometer te verplaatsen—vanop het water naar de bovenste laag—verkleinden we praktisch de barrière voor de reactie met de helft,” zei Dr. Christoph Schran, hoofd van de FAST-groep aan het Cavendish Laboratory, die het onderzoek leidde.
“Dat we zulke drastische veranderingen tijdens de initiële diffusiefase van de reactie observeerden, was opmerkelijk. Het deed ons afvragen: is er een ander fundamenteel proces dat onderhevig is aan zulke veranderingen? Welke andere reactiemechanismen kunnen we ontdekken?”
Het onderzoeksteam is nu van plan hun modellering uit te breiden om andere soorten zoals natrium-, chloride- en carbonaat-ionen, die overvloedig aanwezig zijn in de oceanen van de aarde, op te nemen. Dit zal een verdere laag van realisme aan hun simulaties toevoegen, wat zal helpen bij de nauwkeuriger voorspelling van pH-trends en oppervlakreactiviteit.